 更新时间:2026-04-06
更新时间:2026-04-06 点击次数:
点击次数:
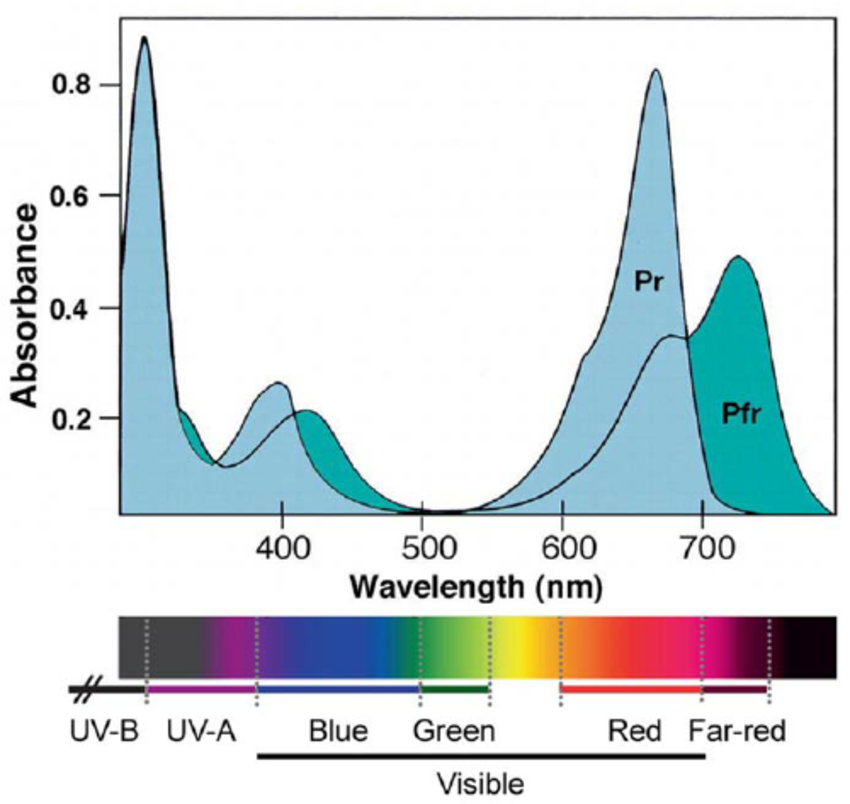
1 、紫外可见光: 波长范围: 200-800 nm. (1)紫外光区: 200-400nm (2)可见光区:400-800nm 2. 紫外-可见光谱: 利用被测物质的分子对紫外-可见光选择性吸收的特性而建立起来的方法。*紫外可见光波长短,能量高,与分子相互作用引起分子中三种能级跃迁。表现为带光谱紫外可见吸收光谱 紫外可见光谱曲线采用连续光源照射,记录吸收后光谱曲线。表示方法: A- ?特性参数: ? max →最大吸收波长:吸收强度最大处对应的波长。? max →在最大吸收波长的摩尔吸光系数。二、紫外可见光谱产生机理 ultraviolet spectrometry pounds (1)有机化合物分子中电子类型: σ电子、π电子、 n电子。 COH n??H (2)轨道类型: 分子轨道理论:成键轨道—反键轨道。分子轨道有σ、σ*、π、π*、 n 5 种, 能量高低σπnπ*σ* (3)、跃迁方式: 当紫外可见光照射分子时电子吸收紫外或可见辐射后,就从基态向激发态(反键轨道)跃迁。理论上有六种σ→σ*;σ→π*;π→σ*;π→π* n →σ*; n→π*实际观察主要有四种跃迁,所需能量ΔΕ大小顺序为: σ→σ*? n→σ*?π→π*? n→π* 1)、σ→σ*跃迁特点: 所需能量最大; σ电子只有吸收远紫外光的能量才能发生跃迁; 饱和烷烃的分子吸收光谱出现在远紫外区; 吸收波长λ200 nm ; 例:甲烷的λ max 为 125nm , 乙烷λ max 为135nm 。只能被真空紫外分光光度计检测到; 一般作为溶剂使用; 2)、 n→σ*跃迁含有杂原子(N 、 O 、 S 、P、X)的饱和有机化合物, 会发生 n→σ*跃迁, 吸收的波长在 200nm 附近,大多数化合物仍在小于 200nm 区域内随杂原子的电负性不同而不同,一般电负性越大,电子被束缚得越紧,跃迁所需的能量越大,吸收的波长越短。 CH3Cl :? max=173nm , CH3Br :? max= 204nm , CH3I 的为? max= 258nm 。 n —σ*跃迁所引起的吸收,摩尔吸光系数一般不大?=100 ~300 3)、π→π*跃迁是π电子从成键π轨道向反键π* 轨道的跃迁,含有π电子基团的不饱和有机化合物,都会发生π—π*跃迁特点: 跃迁所需能量比σ→σ*跃迁小。若无共轭,与 n →σ* 跃迁差不多。 200nm 左右; 若有共轭体系,波长向长波方向移动,波长在 200~700 nm 吸收强度大, ?在 10 4 ~10 5范围内,强吸收含不饱和键的化合物发生π→π*跃迁 C=O , C=C, C ≡C (1)单烯烃π→π*跃迁乙烯π→π*跃迁的λ max 为162nm ,ε max 为: 1 104 L mol-1 cm -1。 cc HH HHλ max ε max 1-己烯 177 104 - 己二烯 178 2 104